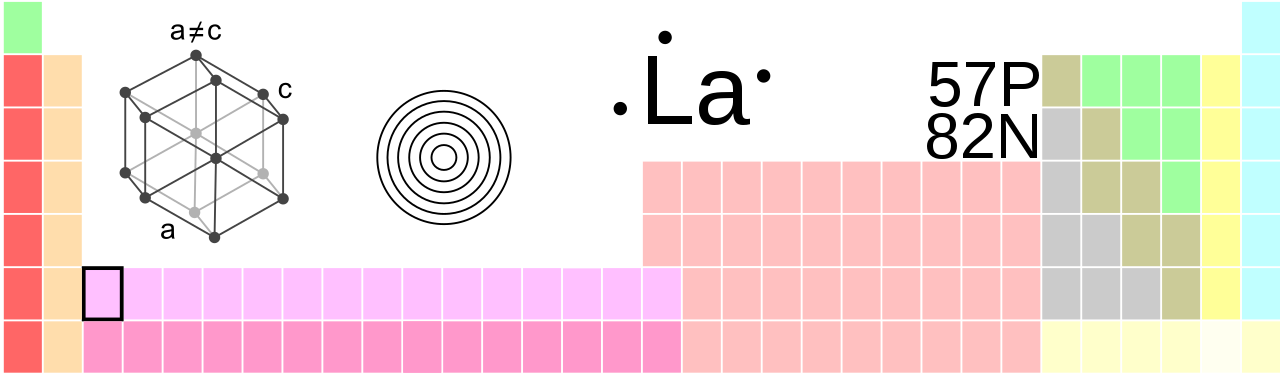
Lantânio, La, número atômico 57
geral
Lantânio [lantaːn] é um elemento químico com o elemento símbolo La e o número atômico 57. Pertence aos metais de transição, bem como aos metais das terras raras, na tabela periódica está no 6. Período e o 3. Subgrupo (grupo 3) ou grupo escândio. Principalmente, ele também é contado para os Lanthanoiden, mesmo que a f-shell do elemento esteja desocupada.
Lantânio (em grego: λανθάνειν, lanthanein, "a ser escondido") 1839 foi descoberto pelo químico e cirurgião sueco Carl Gustav Mosander. De um nitrato de cério supostamente puro, ele ganhou por cristalização fraccionada de sulfato de lantânio.
O lantânio ocorre naturalmente apenas em compostos químicos associados a outros lantanídeos em vários minerais. Principalmente estes são:
Monazita ((Ce, La, Th, Nd, Y) PO4)
Bastnäsit ((Ce, La, Y) CO3F)
recuperação
Após uma separação complexa do outro companheiro de lantanídeo, o óxido é reagido com fluoreto de hidrogênio ao fluoreto de lantânio. Posteriormente, isso é reduzido a lantânio com cálcio para formar fluoreto de cálcio. A separação dos resíduos de cálcio remanescentes e impurezas ocorre em uma refusão adicional in vacuo.
Características
O metal branco prateado é maleável e dúctil. Existem três modificações metálicas.
O lantânio é indigno. Ele rapidamente se torna revestido com uma camada de óxido branco no ar, que reage no ar úmido do hidróxido.
Em temperaturas acima de 440 ° C, o lantânio queima a óxido de lantânio (La2O3). A formação de hidrogênio em água fria é lenta, em água morna uma reação rápida ao hidróxido.Em ácidos diluídos, o lantânio se dissolve sob a evolução do hidrogênio.Com muitos elementos, reage diretamente no calor, com halogênios, mesmo à temperatura ambiente. O lantânio e o hidrogênio formam um hidreto não estequiométrico preto sensível à água.
Usar
O lantânio é um componente do misch metal. Os materiais de sílex pirofóricos contêm 25 a 45 por cento em peso de lantânio. Além disso, encontra uso como agente redutor na metalurgia. Como uma adição de ferro fundido, suporta a formação de grafite esferoidal, como um aditivo de liga, melhora a resistência à oxidação. As misturas de lantânio reduzem a dureza e a sensibilidade à temperatura do molibdênio.
Catodos de alta qualidade para gerar elétrons livres consistem em hexaboreto de lantânio como um substituto para o fio de tungstênio. O óxido de lantânio de alta pureza é utilizado na indústria do vidro para a produção de vidros de alta qualidade com alto índice de refração para a ótica z. B. usado para lentes de câmera.
Com Cobalto:
A liga de cobalto-lantânio LaCo5 é usada como um material magnético, titanato de bário dopado com lantânio para a produção de termistores PTC (resistores dependentes da temperatura). Em conjunto com cobalto, ferro, manganês, estrôncio e outros, serve como cátodo para células a combustível de alta temperatura (SOFC). O níquel de lantânio "contaminado" (LaNi5) é usado como armazenamento de hidrogênio em baterias de armazenamento de níquel metal hidreto. Além disso, ele vem em lâmpadas de arco de carbono para iluminação de estúdio e em sistemas de projeção de filmes (aplicação histórica?) Antes.
Com titânio:
Um metal de liga com composições de material de lantânio e titânio, o efeito é atribuído ao fato de que, com o processamento de formação de cavacos, o comprimento do cavaco é reduzido. Isso deve facilitar o processamento do metal.
No campo da medicina, instrumentos resistentes à corrosão e facilmente esterilizáveis são produzidos a partir do metal de liga. Diz-se que esta liga de metal à base de titânio é particularmente adequada para ferramentas e aparelhos cirúrgicos, porque a propensão para alergia de usar essa liga de metal com titânio relativamente a outras ligas deve ser baixa.
Como óxido de lantânio
Produção de óculos (Lanthanglas) com índice de refração comparativamente alto, que por sua vez muda apenas ligeiramente com o comprimento de onda (baixa dispersão), para câmeras, lentes telescópicas e para lentes de óculos
Produção de cristais e manchas de porcelana. Substitui compostos de chumbo mais tóxicos com melhoria simultânea da resistência química (melhoria da resistência do álcali, "máquina de lavar louça segura")
Catalisação de zeólitas durante o craqueamento catalítico em fluido na refinaria de petróleo
Produção de massas condensadoras de cerâmica e vidros sem silicato
Componente de polidores de vidro
Produção de catodos quentes para tubos de elétrons (também boratos de lantânio)
Como carbonato de lantânio
Medicamento para baixar o nível de fosfato em pacientes em diálise (o chamado aglutinante de fosfato)
O lantânio é classificado como de baixa toxicidade. Uma dose tóxica é desconhecida. No entanto, o pó de lantânio é considerado altamente corrosivo porque reage muito facilmente, por exemplo, pela hidratação da pele, ao hidróxido de lantânio básico (semelhante aos elementos cálcio e estrôncio). A dose letal em ratos é 720 mg.
| Geral | |
| Nome, symbolOrder number | Lantânio, La, 57 |
| série | metais de transição |
| Grupo, período, bloco | 3, 6, d |
| Aparência | branco prateado |
| número CAS | 7439-91-0 |
| Fração de massa do envelope da terra | 17 ppm |
| nuclear | |
| massa atômica | 138,9055 u |
| raio atômico | 195 pm |
| Raio covalente | 207 pm |
| Elektronenkonf. | [Xe] 5d (1) 6s2 |
| 1. ionização | 538,1 KJ / mol |
| 2. ionização | 1067 KJ / mol |
| 3. ionização | 1850 KJ / mol |
| fisicamente | |
| estado físico | fest |
| estrutura de cristal | hexagonal |
| densidade | 6,17 g / cm3 (20 ° C) |
| magnetismo | paramagnético (χm = 5,4 * 10 (-5)) |
| ponto de fusão | 1193 K (920 C) |
| ponto de ebulição | 3743 K (3470 C) |
| Volume molar | 22,39 * 10 (-6) m (3) / mol |
| Calor de vaporização | 400 KJ / mol |
| calor de fusão | 6,2 KJ / mol |
| Condutividade elétrica | 1,626 * 10 (6) A / (V * m) |
| condutividade térmica | 13 W / (m * K) |
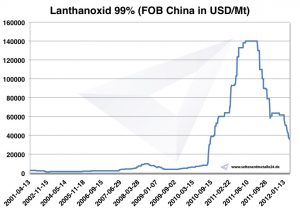
Preço de lantânio