Ítrio, Y, número atômico 39
geral
Ítrio [ʏtriʊm] é um elemento químico com o símbolo Y e o número ordinal 39. Pertence aos metais de transição e aos metais terras raras, na tabela periódica que está no 5. Período, bem como o 3. Subgrupo (grupo 3) ou grupo escândio. O ítrio tem o nome do primeiro local, a mina de Ytterby, perto de Estocolmo, assim como o itérbio, o térbio e o érbio.
O ítrio (de Ytterby, meu perto da capital sueca, Estocolmo) foi descoberto por Johan Gadolin 1794 em Mineral Ytterbit. A 1824 fabricou o contaminante Friedrich Wöhler, reduzindo o cloreto de ítrio com potássio. Apenas 1842 sucedeu a Carl Gustav Mosander separando o ítrio dos elementos de acompanhamento érbio e térbio.
O ítrio não é encontrado na natureza no estado elementar. Os minerais contendo ítrio (Yttererden) estão sempre associados a outros metais de terras raras. Também pode estar contido em minérios de urânio. Areias monazíticas com até 3% ítrio e bastnasita com 0,2% ítrio são comercialmente degradáveis. Além disso, é o principal constituinte da xenotima (Y [PO4]).
Grande Monazitvorkommen, o começo do 19. Descobertos e explorados no Brasil e na Índia no século 20, esses dois países se tornaram grandes produtores de minérios de ítrio. Apenas a abertura da Mina de Mountain Pass na Califórnia, que produziu grandes quantidades de bastnasite até as 1990s, fez dos EUA o principal produtor de ítrio, embora o bastnasite ali extraído contenha apenas uma pequena quantidade de ítrio. Desde o fechamento desta mina, a China é o maior produtor de terras raras da 60%. Estes são obtidos em uma mina perto de Bayan Kuang, cujo minério contém xenotima, e de minerais de argila que absorvem íons, que são extraídos principalmente no sul da China.

Metal ítrio
recuperação
A separação das terras raras umas das outras é um passo trabalhoso na produção de ítrio. A cristalização fracionada de soluções salinas foi o método preferido no início, que foi usado cedo para a separação em escala de laboratório das terras raras. Somente a introdução da cromatografia iônica tornou possível separar as terras raras em escala industrial.
O óxido de ítrio concentrado é convertido em flúor. A redução subsequente ao metal ocorre com o cálcio no forno de indução a vácuo.
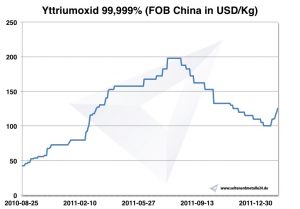
Óxido de ítrio de gráfico 2010-2011
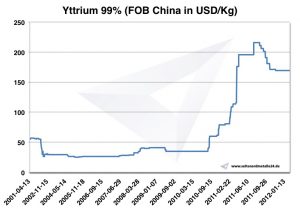
Gráfico Ítrio 2001-2012
Características
O ítrio é relativamente estável no ar, mas escurece sob a luz. Em temperaturas acima de 400 ° C, interfaces novas podem se inflamar. O ítrio finamente dividido é relativamente instável. O ítrio tem uma seção transversal de baixa captura para nêutrons.
É principalmente trivalente em seus compostos. No entanto, também existem compostos de cluster nos quais o ítrio pode assumir estados de oxidação <3.
Há um total de isótopos 32 entre 76Y e 108Y, bem como outros isómeros centrais 24 conhecidos. Destes, apenas um 89Y, do qual o ítrio natural existe exclusivamente, é estável. O ítrio é um dos elementos puros 22. Os radioisótopos mais estáveis são 88Y com uma semi-vida de 106,65 dias e 91Y com uma semi-vida de 58,51 dias. Todos os outros isótopos têm uma semi-vida inferior a um dia, à excepção de 87Y, que tem uma semi-vida de 79,8 horas, e 90Y com 64 horas. Os isótopos de ítrio estão entre os produtos mais comuns da fissão de urânio em reatores nucleares e em explosões nucleares.
Tabela Periódica ítrio-39
Usar
Ítrio metálico é usado na tecnologia de reator de tubo. Uma liga de ítrio-cobalto pode ser usada como um ímã permanente. O ítrio é usado como material para aquecimento de fios em fontes iônicas de espectrômetros de massa. Na metalurgia, pequenos aditivos de ítrio são usados para refino de grãos, por exemplo, em ligas condutoras de calor de ferro-cromo-alumínio, cromo, molibdênio, titânio e ligas de zircônio. Em ligas de alumínio e magnésio, tem um efeito fortalecedor. Tecnicamente mais importantes são os compostos de ítrio oxídico:
Nitrato de ítrio como material de revestimento em um manto
Granada de ítrio e alumínio (YAG) serve como cristal laser
Granada de ferro ítrio (YIG) como filtro de microondas
Zircônia estabilizada com ítrio como eletrólito sólido em células a combustível (SOFC, célula a combustível de óxido sólido)
No entanto, o uso mais importante de ítrio e Yttriumoxidsulfide são as diversas aplicações em európio trivalente (vermelho) e túlio (azul) Fósforos dopados (fósforos) em tubos de imagem de televisão, lâmpadas fluorescentes e tubos de radar.
Além disso, as cerâmicas e ligas de ítrio são utilizadas em:
sondas lambda
Supercondutores (por exemplo, óxido de cobre-bário-ítrio YBa2Cu3O7-x)
ligas ODS
faísca
Como emissor beta puro, o 90Ytrium é utilizado em medicina nuclear para terapia, por exemplo, Radiosynoviorthese.
O ítrio é considerado não essencial e tóxico (valor MAK = 5 mg / m3).
| Geral | ||
| Nome, símbolo
ordinal |
Ítrio, Y, 39 | |
| série | metais de transição | |
| Grupo, período, bloco | 3, 5, d | |
| Aparência | branco prateado | |
| número CAS | 7440-65-5 | |
| Fração de massa do envelope da terra | 26 ppm | |
| nuclear | ||
| massa atômica | 88,90585 u | |
| raio atômico | 180 pm | |
| Raio covalente | 190 pm | |
| Elektronenkonf. | [Kr] 4d (1) 5s2 | |
| 1. ionização | 600 KJ / mol | |
| 2. ionização | 1180 KJ / mol | |
| 3. ionização | 1980 KJ / mol | |
| fisicamente | ||
| estado físico | fest | |
| estrutura de cristal | hexagonal | |
| densidade | 4,472 g / cm3 | |
| magnetismo | paramagnético (χm = 1,2 * 10 (-4)) | |
| ponto de fusão | 1799 K (1526 C) | |
| ponto de ebulição | 3609 K (3336 C) | |
| Volume molar | 19,88 * 10 (-6) m (3) / mol | |
| Calor de vaporização | 380 KJ / mol | |
| calor de fusão | 11,4 KJ / mol | |
| Condutividade elétrica | 1,66 * 10 (6) A / (V * m) | |
| condutividade térmica | 17 W / (m * K) | |
