Bismuto, Bi, número atômico 83
Bismuto - história, ocorrência, extração, usos e preços do bismuto
O bismuto ou bismuto (obsoleto também: bismuto) é um elemento químico com o elemento símbolo Bi e o número atômico 83. Na tabela periódica está no 5. Grupo principal ou grupo nitrogênio.
Não há isótopo estável conhecido. No entanto, a extremamente baixa meia vida extremamente baixa radioatividade do 209Bi que ocorre naturalmente é irrelevante para uso prático. A radioatividade pôde ser detectada apenas 2003, uma vez que anteriormente os métodos altamente sensíveis necessários para medição não estavam disponíveis; O 1990Bi foi considerado o nuclídeo estável mais pesado nos anos 209.
História
Como um elemento separado, o bismuto tornou-se o centro do 18. Century pelos químicos Claude François Geoffroy, Johann Heinrich Pott, Carl Wilhelm Scheele e Torbern Olof Bergman demonstraram. Anteriormente, era frequentemente considerado como um derivado de chumbo, estanho, antimônio e outros metais ou minerais. No livro Um livro de montanha útil (sobre 1527), o minério de bismuto (wissmad arzcz) é mencionado como um companheiro de minério de prata. Mais tarde no 16. O século Georgius Agricola tentou uma distinção mais precisa.
O nome do metal, que aparece como wesemut no alemão 1390 e lat 1450 como wismutum, 1530 como bisemutum, pode ser encontrado na tradução em árabe do Dioscuri de 9. Século documentado formulário b [i] sīmūtīyūn ser atribuído, o que é em si provavelmente uma transliteração do grego antigo ψιμύθιον psimýthion, branco de chumbo 'representa. A gênese do árabe ṯmid, antimônio 'também foi adotada; Muitas vezes, além do suposto primeiro motim na mina St. Georgen nos prados perto de Schneeberg no Erzgebirge em 15. Century, ou na variant wis (se) mat. que significa "massa branca".
O símbolo químico Bi foi sugerido por JJ Berzelius no ano 1814.
ocorrência
O bismuto ocorre naturalmente na natureza, que é na forma elementar, e é reconhecido como um mineral pela Associação Mineralógica Internacional (IMA). O 9 usado pelo IMA. Edição da classificação de minerais após Karl Hugo Strunz lidera o bismuto juntamente com antimônio, arsênico e stibarsen na subdivisão dos elementos arsênico sob o sistema não. 1.CA.05 (edição 8 obsoleta: I / B.01-40). No predominantemente utilizado em classificação de língua inglesa de minerais de acordo com Dana Bismuth pertence ao "grupo arsênico" com o sistema não. 01.03.01.
O bismuto sólido é formado em veios hidrotermais de pegmatitos e veios de quartzo de estanho-tungstênio contendo topázios e geralmente junto com vários minérios de cobre, níquel, prata e estanho. O bismuto raramente desenvolve formas cristalinas bem formadas, mas pode atingir um tamanho de até 12 centímetros. É geralmente encontrado na forma de agregados dendríticos, laminares ou granulares, mas também como gêmeos polissintéticos com estriações paralelas ("bismuto de primavera") ou superfícies laterais em forma de funil, desenhadas no centro de cristal.
(Como 2011) Até agora, cerca de 1400 localidades para bismuto dignas são considerados conhecida. Os sites são principalmente na Austrália, Bolívia, China, Canadá, México, Peru e Espanha, historicamente Bieber em Spessart e no Erzgebirge onde bismuto (tanto na forma pura e como sulfeto (Bismuthinit) seleneto (Selenidbismutglanz) e óxido Bismit) é encontrado. Além disso trata de bismuto, bem como antimónio e arsénio, por vezes como um sulfureto dupla antes: Galenobismutit (PbBi2S4) Lillianit (Pb3Bi2S6) Silberbismutglanz (AgBiS2) Kupferbismutglanz (CuBiS2) e Kupferbismutblende (Cu6Bi2S6). é conhecido também um sulfureto de telúrio na forma de Tellurbismut (Bi2Te2S) e um silicato chamado Eulytin (Bi4 (SiO4) 3).
No geral, são conhecidos o bismuto sólido em torno dos minerais de bismuto 230.
Extração e apresentação
Para a produção de bismuto, pode-se assumir minérios oxídicos ou sulfídicos.
Os minérios de óxidos são reduzidos a bismuto em fornos a carvão:
Os sais de sulfureto de bismuto podem ser reduzidos com ferro pelo método de precipitação:
Ou os minérios sulfídicos são primeiramente convertidos em óxidos e depois reduzidos com carvão (método de redução de Röder):
O bismuto cru é então removido por fusão oxidante de outros elementos (antimônio, arsênico, chumbo, ferro e enxofre). O cobre é removido por fusão com sulfeto de sódio, ouro e prata por extração de bismuto fundido com estanho.
Propriedades
Propriedades físicas
O bismuto é um metal ou semi-metal prateado branco, frágil e grosseiramente cristalino com um toque de rosa. Tem uma estrutura cristalina romboédrica com bicamadas muito densas. A menor distância entre duas camadas duplas é 352,9 pm, que é apenas 15% maior que a menor distância entre dois átomos dentro de uma camada dupla. Monocristais de bismuto apresentam pronunciada clivagem paralela a essas bicamadas.
O bismuto tem o efeito Hall mais forte de todos os elementos do tipo metal e como um semi-metal na forma pura, uma condutividade elétrica pobre. Ele mostra - além de supercondutores e grafite pirolítica - além da propriedade diamagnética mais forte, é empurrado para fora de um campo magnético aplicado externamente. O efeito Schubnikow-de-Haas (oscilações de resistência elétrica em um campo magnético externo) foi observado pela primeira vez em cristais de bismuto e medido. Antes do desenvolvimento de sensores Hall e placas de campo, a chamada espiral de bismuto, uma bobina com fio de bismuto isolado e fino, foi usada para medir campos magnéticos. A mudança de resistência da bobina sob a influência de um campo magnético variável foi certamente muito pequena em comparação com os sensores atuais.
Existem duas modificações conhecidas do bismuto: o bismuto, que é comum à temperatura ambiente, forma uma estrutura cristalina cúbica centrada no corpo sob alta pressão (a partir do 9 GPa).
O bismuto líquido se expande como uma das poucas substâncias quando se solidifica (anomalia de densidade). Este fenômeno também é observado em gálio, germânio, plutônio, silício, telúrio e água. É baseado no bismuto que ocorre uma transição de fase dupla durante a fusão (e solidificação): uma vez a transição de fase 1. Encomende de sólido para líquido (geralmente com pequena diminuição na densidade) e, além disso, uma transição de fase 1. Ordem de metalóide a metal com aumento significativo na densidade, o que também explica a entropia incomumente grande de fusão de 21,1 J / (K · mol) e o súbito aumento na condutividade elétrica do fundido de bismuto.
Propriedades químicas
O bismuto é resistente ao ar seco a temperatura normal. No ar úmido, no entanto, uma camada de óxido se forma na superfície. Além disso, o bismuto é resistente à água e a ácidos não oxidantes (ácido clorídrico e ácido sulfúrico diluído). Em ácidos oxidantes (ácido nítrico ou ácido sulfúrico concentrado quente) o bismuto é dissolvido para formar sais de bismuto (BiX3). Em forma de pó, é um sólido inflamável, pode ser facilmente inflamado por uma breve exposição a uma fonte de ignição e continua a queimar após a remoção. O risco de ignição é maior, quanto mais fina a substância é distribuída. O metal em uma forma compacta não é inflamável.
Quando em brasa, o bismuto queima com uma chama azulada a uma fumaça marrom-amarelada - óxido de bismuto (III) (Bi2O3).
Sob o calor, o bismuto combina diretamente com os halogênios, bem como com enxofre, selênio e telúrio diretamente. O bismuto não reage com nitrogênio e fósforo.
isótopo
O bismuto natural consiste apenas do isótopo 209Bi. Em 2003 foi apresentado no Instituto de Astrofísica espacial firmemente em Orsay (França) que este isótopo anteriormente considerado estável um emissor alfa com uma meia-vida de (1,9 0,2 ±) · 1019 anos (cerca de 19 quintilhões de anos). O decaimento muito lento de 209Bi em 205Tl justificado por um lado, pela proximidade com a 208Pb isótopo duplamente mágica no esquema eo fato de que a própria 209Bi é apenas mágico. A meia-vida longa resulta em uma atividade de 0,0033 Bq / kg (correspondendo a um único decaimento nuclear por cinco minutos e quilogramas).
209Bi é o penúltimo membro da série Neptunium e, exceto 205Tl, o único que ainda é natural. Como os nuclídeos que estão no início da série Neptunium estão agora sendo incubados em reatores nucleares, a quantidade de 209Bi na Terra está aumentando com o tempo.
Usar
O bismuto é utilizado como componente de liga em ligas de baixo ponto de fusão, por exemplo, para o metal de Wood, que funde a 70 ° C, para o metal de Rose com ponto de fusão de 98 ° C e para o metal de Lipowitz, que funde a 60 ° C.
Uso técnico
A liga Bismanol com manganês é um forte ímã permanente.
No revestimento de ligas (estanhamento por imersão a quente) para conectores solares, serve como um substituto para o chumbo.
Os cristais simples de bismuto sintético com dimensões superiores a 20 centímetros e placas de bismuto policristalino são utilizados como filtros de nêutrons para investigações de materiais em reatores de pesquisa.
O teleureto de bismuto composto químico bombeia energia para os elementos Peltier.
O material de mudança de fase de alguns DVD-RAM contém bismuto, consulte Tecnologia de mudança de fase.
O bismuto é propagado por algumas fontes como um elemento de liga em aços de corte livre para substituir o chumbo. Deve melhorar a usinabilidade destes aços sem as propriedades ecológicas negativas do chumbo. Do ponto de vista da metalurgia do aço, no entanto, isso é desfavorável, uma vez que o bismuto praticamente não pode ser removido metalurgicamente e, em seguida, aparece como um elemento de acompanhamento indesejável nos aços produzidos a partir da sucata. Na indústria eletrônica, uma liga de estanho de bismuto é usada como um substituto (palavra-chave RoHS) para soldas com chumbo. A desvantagem é que, para o estanho Bismuto, é necessário um equipamento de solda próprio. Contaminação com chumbo (por exemplo, reparo de equipamentos antigos) resulta em um ponto de fusão muito baixo, enquanto o uso de ferramentas de liga de estanho-prata leva a altas temperaturas e contaminação da ferramenta de bismuto.
O óxido de bismuto é utilizado para a produção de vidros ópticos, bem como auxiliares de sinterização em cerâmica técnica. Ele também encontra aplicação na forma de bismuto germanato como um detector de cintilação em tomografia por emissão de pósitrons (PET).
Uma liga de chumbo-bismuto foi usada na União Soviética como um refrigerante para reatores nucleares. Embora mais eficaz do que o resfriamento por água pressurizado convencional, esta liga também é mais difícil de manusear. A liga solidifica a uma temperatura abaixo de 125 ° C e pode então causar grandes danos ao reator. Tais reatores foram utilizados, entre outros, em submarinos nucleares (por exemplo, classe submarina Alfa).
O bismuto também é usado como um substituto de chumbo não-tóxico para munição de espingarda. No entanto, isso não é muito comum.
No 16. Century desenvolveu no sul da Alemanha e na Suíça uma técnica de pintura na qual o bismuto era usado como revestimento de caixas ou caixas decorativas menores, em parte também para altares de madeira. Essa técnica é chamada de pintura de bismuto.
Use na indústria química
O óxido de cloreto de bismuto (BiOCl) é usado como um pigmento perolado branco-prateado em cosméticos.
O vanadato de bismuto é usado como um pigmento amarelo esverdeado altamente resistente ao clima em uso e encontra z. B. em tintas de alta qualidade, tintas de emulsão para uso de fachadas, plásticos e tintas de impressão.
Além disso, o bismuto é usado como catalisador na indústria química.
Uso médico
compostos de bismuto tais como Dibismut-tris (tetraoxodialuminat), oxynitrate bismuto (subnitrato de bismuto, nitrato de bismuto básico) encontrado como um componente da terapia com antibiótico contra o agente patogénico Helicobacter pylori utilização, o que pode causar no estômago e úlceras do duodeno (erradicação). A aplicação é uma chamada terapia quádrupla (terapia combinada de um inibidor da bomba de prótons e uma terapia tripla com bismuto [sal de bismuto, tetraciclina, metronidazol).
Os compostos de bismuto também são parcialmente usados na diarréia como adstringentes e redutores de odor no mau hálito e na flatulência. Além disso, alguns compostos (por exemplo, Bibrocathol) são utilizados como anti-séptico.
Além disso, o bismuto é usado diagnosticamente na tomografia por emissão de pósitrons na forma de bismuto-germanato como material detector do aparelho de tomografia.
Historicamente, o bismuto estava no final do 19. Século como parte de feridas em pó (por exemplo, Dermatol) usado. Desde os anos 1920, tem sido usado como um remédio para a sífilis. No entanto, foi completamente substituído por antibióticos modernos.
Os sais de bismuto também têm sido usados como agentes de contraste de raios-X para visualizar o trato gastrointestinal (a chamada refeição de bismuto). Aqui, o sal de bismuto foi substituído por sulfato de bário.
Galato de bismuto é usado em uma formulação de pomada de pele de Stolte, e a pomada pode ser usada para tratar a pele inflamatória em bebês.
envenenamento
O envenenamento por bismuto (bismuto) é raro devido à má absorção no trato gastrointestinal. É em grande parte semelhante ao envenenamento por mercúrio. Típico são a aparência de uma cinza de ardósia para Bismutsaums pretas (bismuto deposição de sulfureto) sobre a mucosa oral, com formação de mucosite oral (estomatite) e gengivite (com afrouxamento dos dentes, falhas), inflamações intestinais (enterite) com diarreia e danos nos rins (Bismutnephropathie).
prova
O bismuto é detectado pela rampa de bismuto com tioureia. Fluoreto de sódio, cloreto de sódio e tartarato de potássio e sódio são usados para precipitar íons interferentes indesejáveis:
NaF para a complexação de Fe3 + e Al3 +
NaCl para a precipitação de Ag + e Hg22 +
Tartarato para a complexação de Sb3 + e Sn2 +
Na presença de Bi3 +, forma-se um complexo de tioureia cristalino, amarelo-limão, no qual três moléculas de tioureia estão associadas ao bismuto via enxofre:
![{\displaystyle {\ce {\rm {Bi^{3+}{+}3SCN2H4{->}[Bi(SCN2H4)3]^{3+}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c283de06adc520701a39cebdb2d9f9e206572f68)
Reações de detecção alternativas:
Em uma reação redox com íons de estanho (II) como agente redutor, o bismuto elementar precipita-se em preto.
Com solução de iodeto de sódio: precipita primeiro iodeto de bismuto (III) preto, que depois se dissolve em excesso de iodeto como um complexo tetraiodobismutato laranja:
![{\ displaystyle {\ ce {\ rm {Bi ^ {3 +} {+} 4I ^ {-} {->} [BiI4] ^ {-}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8f1a3e20448941130afb1ebcb56f6ed3bd093dad)
O 1,3,4-tiadiazole-2,5-ditiol também é adequado como um agente complexante para detecção.
Conexões
O bismuto é principalmente trivalente, mas há também um e bismuto pentavalente; No entanto, o óxido de bismuto (V) é um agente oxidante muito forte que oxida mesmo o manganês (II) ao permanganato. Também forma cátions poliméricos. É estável no ar.
- compostos oxigenados
Óxido de bismuto (III) (bismuto, também chamado de fezes de bismuto) - compostos de enxofre
De bismuto (III), sulfureto - compostos de hidrogénio
Hidrogênio de bismuto (bismuto) - Haletos e nitratos
Fluoretos: fluoreto de bismuto (III), fluoreto de bismuto (V), fluoreto de óxido de bismuto
Cloretos: subcloreto de bismuto, cloreto de bismuto (III), óxido de cloreto de bismuto
Brometo: subbrometo de bismuto, brometo de bismuto (III), brometo de óxido de bismuto
Iodetos: iodeto de bismuto (I), iodeto de bismuto (III), iodeto de óxido de bismuto
Nitratos: nitrato de óxido de bismuto (subnitrato de bismuto) - Como anião
bismutato de sódio (V)
Preços, gráficos, histórico de preços
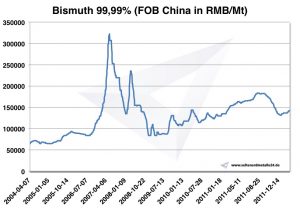
Gráfico Bismuto 2004 2011



