Tântalo, Ta, número atômico 73
Preço, ocorrência, extração e uso de tântalo
Tântalo [ˈtântalo] é um elemento químico com o símbolo Ta e o número atômico 73; na tabela periódica, está no quinto subgrupo ou grupo do vanádio. É um metal de transição brilhante, dúctil, cinza-grafite que ocorre raramente. O tântalo é usado principalmente para capacitores com alta capacitância e ao mesmo tempo de tamanho pequeno. Como o metal não é tóxico e é inerte aos fluidos corporais, ele também é usado para implantes, por exemplo, como prego ósseo.
O elemento foi descoberto em 1802 por Anders Gustav Ekeberg em um minério de columbita finlandês. Ele separou um óxido muito estável (óxido de tântalo (V)) que não se dissolveu em nenhum ácido. Tem o nome de Tântalo, uma figura da mitologia grega. De acordo com Ekeberg, a razão desse nome é que o próprio óxido permanente "tem que definhar e não pode matar sua sede, como Tântalo no mundo subterrâneo".
Quase ao mesmo tempo, Charles Hatchett encontrou algo muito semelhante em um minério colombiano columbium. Os dois elementos eram considerados idênticos até 1844, quando Heinrich Rose reconheceu que dois elementos diferentes estavam presentes nos minérios de columbita, ou seja, o tântalo e o columbio. Ele chamou o último de nióbio.
Após a descoberta do novo elemento, vários químicos tentaram representar o tântalo na forma elementar. O primeiro a produzir tântalo elementar reduzindo o fluoreto de tântalo com potássio foi Jöns Jakob Berzelius em 1815. No entanto, como o tântalo representado por Rose, seu metal era apenas 50% de tântalo. Em 1902, Henri Moissan tentou produzir tântalo em um forno elétrico, mas o carbono que ele continha tornava seu produto muito duro e quebradiço.
O primeiro que conseguiu produzir tântalo dúctil puro foi Werner von Bolton em 1903. Ele conseguiu isso reduzindo os óxidos brilhantes no vácuo e derretendo metal impuro de tântalo no vácuo e usando um arco elétrico de chama.
A primeira aplicação do novo elemento foi como filamento de lâmpadas. O motivo da mudança do ósmio usado anteriormente para o tântalo foi que ele é mais fácil de processar e tem uma temperatura de uso mais alta possível, de até 2300 ° C. Posteriormente, foi substituído por tungstênio, que tem um ponto de fusão ainda mais alto e, portanto, permite um espectro de luz mais próximo ao da luz solar e uma saída de luz maior.
Em 1922, uma nova aplicação foi encontrada para o tântalo com seu uso em retificadores e um ano depois em tubos de rádio.
ocorrência
O tântalo é um elemento raro na Terra, com teor de 2 ppm na crosta continental e 8 ppm na concha terrestre. A frequência é comparável à do arsênio e do germânio. Dentro do grupo, a frequência diminui em uma potência de dez. O tântalo não ocorre naturalmente, mas apenas na forma de seus compostos em vários minerais. Devido à semelhança dos dois elementos, os minérios de tântalo sempre contêm nióbio e vice-versa (socialização). Os minerais mais importantes são os das séries da columbita e da tapiolita, em que vários minerais com a fórmula geral (Mn, Fe2+) (Nb, Ta)2O6 ser resumido. Columbitos de tântalo também são chamados tantalite designado. Exemplos de minerais contendo tântalo nesta série são ferrotapiolita (Fe2+Mn2+) (Ta, Nb)2O6 e tantalita manganês MnTa2O6. Esses minérios são freqüentemente chamados de coltan. Minerais menos comuns são microlita ou toreaulita.
Os principais países produtores de minério de tântalo em 2007 foram a Austrália com 850 toneladas e o Brasil com 250 toneladas. O coltan também é encontrado no Canadá e em vários países africanos, como Etiópia, Moçambique e Ruanda. As ocorrências no leste da República Democrática do Congo, que foram fortemente contestadas na Guerra do Congo de 1996-2008, tornaram-se conhecidas na mídia.
Extração e apresentação
Como o tântalo e o nióbio estão sempre presentes juntos nos minérios usados para extração de tântalo, eles devem ser separados para recuperar os metais puros. Isso é complicado pela grande semelhança dos dois elementos.
O primeiro método de separação foi desenvolvido por Jean Charles Galissard de Marignac em 1866. Ele usou a solubilidade diferente dos dois elementos em ácido fluorídrico diluído. O tântalo forma o K ligeiramente solúvel2TaF7, Nióbio o K bem solúvel3NbOF5 · 2 H2O.
O processo usado tecnicamente hoje é baseado na extração e usa as diferentes solubilidades de sais de flúor complexos em água e certos solventes orgânicos. A mistura de minério é primeiro dissolvida em ácido fluorídrico concentrado ou misturas de ácido fluorídrico e sulfúrico. Os fluoretos complexos [NbOF5]2- e [TaF7]2-. Após a filtração dos constituintes insolúveis, a separação pode ser realizada por extração líquido-líquido com o auxílio de metil isobutil cetona. Se a metil isobutil cetona for adicionada à solução, os complexos de nióbio e tântalo passam para a fase orgânica, enquanto outros elementos, como ferro ou manganês, permanecem na fase aquosa. Quando a água é adicionada à fase orgânica separada, apenas o complexo de nióbio se dissolve nela, o tântalo permanece na metil isobutil cetona.
Com a ajuda de fluoreto de potássio, o tântalo pode ser convertido em um K pouco solúvel2[TaF7] ser derrubado. A redução a tântalo elementar geralmente é feita pelo sódio.
![\ mathrm {K_2 [TaF_7] + 5 \ Na \ longrightarrow Ta + 5 \ NaF + 2 \ KF}](https://upload.wikimedia.org/wikipedia/de/math/4/0/8/4082df7e6f3cde8acd65ddf4230284e5.png)
Redução com sódio
Uma alternativa possível para a extração é a destilação fracionada. Os diferentes pontos de ebulição dos dois cloretos, pentacloreto de nióbio e pentacloreto de tântalo, são usados para esse fim. Estes podem ser extraídos dos minérios com cloro e coque em altas temperaturas. Após a separação, o cloreto de tântalo também é reduzido ao metal com sódio.
Além dos minérios de columbita-tantalita, a escória da fundição de estanho é uma fonte importante para a extração de tântalo (contém uma pequena porcentagem de tântalo).
Propriedades físicas
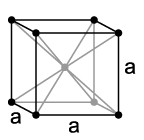
Estrutura cristalina do tântalo,a = 330,3 pm
O tântalo é um metal pesado de alto ponto de fusão distintamente cinza-púrpura, duro como aço (dureza Vickers: 60-120 HV) que é semelhante ao nióbio na maioria de suas propriedades. Ele se cristaliza em uma estrutura de cristal cúbica centrada no corpo. Com um ponto de fusão em torno de 3000 ° C, o tântalo tem o ponto de fusão mais alto de todos os elementos, depois do tungstênio, carbono e rênio. Se apenas uma pequena quantidade de carbono ou hidrogênio for armazenada no metal, o ponto de fusão aumenta significativamente. Com um ponto de fusão de 3880 ° C, o carboneto de tântalo tem um dos pontos de fusão mais altos de todas as substâncias.
O tântalo se torna um supercondutor abaixo de uma temperatura de transição de 4,3 Kelvin.
Embora o tântalo puro seja dúctil e possa ser alongado consideravelmente (resistência à tração: 240 MPa), mesmo pequenas quantidades de carbono ou hidrogênio adicionadas a ele alteram a resistência mecânica significativamente. O material se torna quebradiço e difícil de processar. Este efeito é usado para produzir pó de tântalo. Em tecnologia, ele é carregado com hidrogênio e, portanto, fragilizado, então triturado de acordo e cozido ou liberado do hidrogênio em uma temperatura mais alta.
Propriedades químicas
O tântalo é um metal básico e reage em altas temperaturas com a maioria dos não-metais, como oxigênio, halogênios ou carbono. À temperatura ambiente, entretanto, o metal é protegido por uma fina camada de óxido de tântalo (V) e, portanto, passivado. A reação só ocorre a uma temperatura de cerca de 300 ° C.
Na maioria dos ácidos o tântalo não é solúvel por causa da passivação, nem mesmo a água régia pode dissolver o metal. O tântalo é atacado apenas pelo ácido fluorídrico, oleum (uma mistura de ácido sulfúrico e trióxido de enxofre) e sais fundidos.
isótopo
Há um total de 30 isótopos e 26 isômeros de núcleo de 155Ta up 185Ta conhecido. O tântalo natural consiste quase exclusivamente (99,988%) do isótopo 181Ta. 0,012% do isômero do núcleo também está presente 180mTa antes. Embora isso possa teoricamente ser radioativo, nenhuma decadência foi observada até agora. A meia-vida deve, portanto, exceder 115 Anos.
Usar
A maior parte do tântalo (volume de produção anual mundial de 1.400 t) é usada para capacitores muito pequenos com alta capacitância. Em 2007, 60% do tântalo foi utilizado na fabricação de capacitores. Esses capacitores eletrolíticos de tântalo são usados em toda a microeletrônica moderna, por exemplo, para telefones celulares e na construção de automóveis. O efeito é baseado na camada de óxido de tântalo na superfície da folha de tântalo ferida, que ainda é estável e isola de forma confiável, mesmo em uma versão muito fina. Quanto mais fina a camada entre os eletrodos, maior será a capacitância com a mesma superfície de folha; Além disso, o óxido de tântalo tem uma permissividade extremamente alta, o que também aumenta a capacidade.
Como o tântalo não é tóxico e não reage com tecidos ou fluidos corporais, o tântalo elementar é usado para implantes e instrumentos médicos. Por exemplo, pregos de osso, próteses, braquetes e parafusos de mandíbula são feitos de tântalo. Além disso, é um meio de contraste de raios-X raramente usado devido ao seu alto custo.
Na indústria química, o tântalo é utilizado devido à sua durabilidade. Ele serve como um material de revestimento para vasos de reação e é usado para trocadores de calor e bombas. Para esses fins, o tântalo puro geralmente não é usado, mas ligas que contêm 2,5–10% de tungstênio. São mais estáveis e resistentes do que o tântalo puro. Ao mesmo tempo, a ductilidade desejada é mantida. Outros usos são equipamentos de laboratório, fieiras e cátodos de tubos de elétrons. Aqui, o tântalo se beneficia do fato de ser capaz de absorver até 800 partes em volume de gases a 740 ° C (efeito getter), o que garante um alto vácuo nos tubos.
As superligas usadas na construção de turbinas e motores de aeronaves contêm até 9% de tântalo. Adicionar 3–4% de tântalo a uma superliga de níquel aumenta a resistência do material em altas temperaturas.
segurança
Trabalhar com tântalo e seus compostos normalmente não causa problemas em condições de laboratório. O tântalo elementar e os compostos de tântalo não são tóxicos. No entanto, existem vagas indicações de que alguns compostos de tântalo são cancerígenos. O pó e a poeira de tântalo - como outros metais finamente divididos - representam um alto risco de incêndio e explosão.
Conexões
Óxido de tântalo (V) Ta2O5 é um pó branco usado para fazer óculos de alta refração e materiais especiais de cristal.
O carboneto de tântalo TaC, com sua temperatura de fusão de 3880 ° C e uma dureza quase igual à de um diamante, serve como uma camada protetora em ligas de alta temperatura em motores e ferramentas de corte.
| Geral | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome, símbolo, número atômico | Tântalo, Ta, 73 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| série | metais de transição | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | 5, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | cinza | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| número CAS | 7440-25-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fração de massa da concha de terra | 8 ppm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| nuclear | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| massa atômica | 180,9479 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico (calculado) | 145 (200) pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raio covalente | 138 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| configuração electrónica | [Xe] 4f14 5d3 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionização | 761 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionização | 1500 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| fisicamente | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estado físico | fest | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estrutura de cristal | centrado no corpo cúbico | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| densidade | 16,65 g / cm3 (20 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| dureza de Mohs | 6,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| magnetismo | paramagnético ( = 1,8 10-4) = 1,8 10-4) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ponto de fusão | 3290 K (3017 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ponto de ebulição | 5731 K (5458 ° C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molar | 10,85 · 10-6 m3/ mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de vaporização | 735 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| calor de fusão | 36 kJ / mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| velocidade do som | 3400 m / s em 293,15 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade de calor específico | 140 J / (kg · K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade elétrica | 7,61 · 106 A / (v · m) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| condutividade térmica | 57 W / (m K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Químico | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| estados de oxidação | 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| potencial normais | −0,81 V (½ Ta2O5 + 5 H.+ + 5 e- → Ta + 2½ H2O) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| eletronegatividade | 1,5 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| isótopo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| propriedades de RMN | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| segurança | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Preços de tântalo
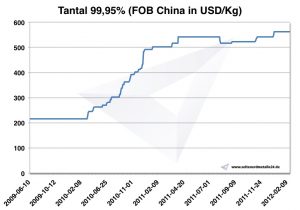
Tântalo de gráfico 2009-2012
Preços atuais de tântalo


