Hafnium é um elemento químico com o símbolo Hf e o número atômico 72. Seu nome vem do nome latino da cidade de Copenhagen, Hafniaem que o elemento foi descoberto. É um metal de transição cinza prateado, brilhante e resistente à corrosão que está no 4º subgrupo (grupo 4) ou grupo titânio na tabela periódica.
O háfnio tem propriedades muito semelhantes às do zircônio diretamente acima dele na tabela periódica. As funções biológicas não são conhecidas, normalmente não ocorre no organismo humano e não é tóxico.
O háfnio foi um dos últimos elementos estáveis da tabela periódica a ser descoberto. A primeira indicação da existência de outro elemento entre o lutécio e o tântalo surgiu da lei de Moseley, fundada em 1912. Em 1914, Henry Moseley tentou encontrar o desconhecido, mas esperado elemento com o número atômico 72 de acordo com essa lei em amostras de minerais de terras raras (hoje lantanídeos). Mas ele não teve sucesso.
Em seu trabalho sobre a teoria atômica publicado em 1922, Niels Bohr previu que a série de lantanídeos com lutécio chegaria ao fim e que o elemento 72 deve, portanto, ser semelhante ao zircônio. O háfnio pôde ser detectado apenas um ano depois: em 1923, em Copenhagen, Dirk Coster e George de Hevesy o descobriram em zircão norueguês usando espectroscopia de raios-X. Uma investigação mais aprofundada de outros minerais mostrou que o háfnio está sempre contido em minerais que contêm zircônio. Jantzen e Hevesy conseguiram separá-los do zircônio cristalizando repetidamente os fluoretos de diamônio e dipotássio dos dois elementos. O háfnio elementar pode então ser obtido por redução com sódio.
ocorrência
O háfnio, com um teor de 4,9 ppm na crosta continental, é um elemento pouco comum na Terra. Em termos de frequência, é comparável aos elementos bromo e césio e mais comum do que os já conhecidos ouro e mercúrio. O háfnio não ocorre naturalmente ou em seus próprios minerais. Minerais de zircônio, como zircão e baddeleita, por outro lado, sempre contêm háfnio; a quantidade de háfnio é geralmente 2% do conteúdo de zircônio (1-5% em peso de háfnio). Um dos poucos minerais que contém mais háfnio do que zircônio é a variedade de zircão Alvit [(Hf, Th, Zr) SiO4].
Análogo ao zircônio, os depósitos de háfnio mais importantes são os depósitos de zircônio na Austrália e na África do Sul. As reservas são estimadas em 1,1 milhão de toneladas (calculadas como óxido de háfnio).
Extração e apresentação
Para obter o háfnio, ele deve ser separado do zircônio. Isso não é possível durante o processo de fabricação, mas ocorre em um processo separado. Os processos de extração são usados para a separação. A solubilidade diferente de certos sais de zircônio e háfnio em solventes especiais é usada. Exemplos disso são as diferentes solubilidades de nitratos em tri-n-butil fosfato e de tiocianatos em metil isobutil cetona. Outras opções de separação possíveis são os trocadores de íons e a destilação fracionada de compostos adequados.
Após o processo de Kroll, o háfnio separado pode primeiro ser convertido em cloreto de háfnio (IV) e depois reduzido a háfnio elementar com sódio ou magnésio.
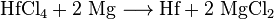
Se um háfnio mais puro for necessário, o processo Van Arkel de Boer pode ser usado. Durante o aquecimento sob vácuo, o háfnio inicialmente reage com o iodo para formar iodeto de háfnio (IV). Este é quebrado novamente em háfnio e iodo em um fio quente.

O háfnio é produzido apenas em pequenas quantidades em uma escala de 100 toneladas. Não é produzido internamente, mas é um subproduto da extração de zircônio sem háfnio para barras de combustível.
Propriedades
Propriedades físicas

Estrutura cristalina de α-Hf, a = 320 pm,c = 505 pm
O háfnio é um metal pesado prateado e brilhante de alta densidade (13,31 g / cm3) Ele se cristaliza em duas modificações diferentes dependendo da temperatura. Em condições normais, ele se cristaliza em um empacotamento hexagonal de esferas (α-Hf) e é, portanto, isotípico a α-Zr, acima de 1775 ° C ele se transforma em uma estrutura cúbica centrada no corpo (β-Hf).
Se a pureza do háfnio for alta, ele é relativamente macio e flexível. É fácil de trabalhar com rolo, forja e martelo. Se, por outro lado, houver traços de oxigênio, nitrogênio ou carbono no material, ele se torna quebradiço e difícil de processar. Os pontos de fusão e ebulição do háfnio são os mais altos do grupo a 2227 ° C e 4450 ° C, respectivamente (ponto de fusão: titânio: 1667 ° C, zircônio: 1857 ° C).
Em quase todas as outras propriedades, o metal se assemelha ao zircônio homólogo mais leve. Isso é causado pela contração dos lantanídeos, que resulta em raios atômicos e iônicos semelhantes (raios atômicos Zr: 159 pm, Hf: 156 pm). Uma exceção é a densidade do zircônio com 6,5 g / cm3 tem um valor significativamente inferior. Uma diferença tecnicamente importante é que o háfnio pode absorver nêutrons 600 vezes melhor. Esta é a razão pela qual o háfnio deve ser separado para uso do zircônio em usinas nucleares.
O háfnio é supercondutor abaixo da temperatura de transição de 0,08 K.
Propriedades químicas
O háfnio é um metal básico que reage com o oxigênio para formar dióxido de háfnio quando aquecido. Outros não metais, como nitrogênio, carbono, boro e silício, também formam compostos nessas condições. Uma densa camada de óxido se forma rapidamente à temperatura ambiente, o que torna o metal passivo e o protege de oxidação posterior.
O háfnio é estável na maioria dos ácidos por causa de sua passivação em condições normais. Corrói-se rapidamente em ácido fluorídrico; a corrosão perceptível ocorre em ácido sulfúrico e fosfórico concentrado quente. As misturas de ácido clorídrico e ácido nítrico, incluindo água régia, devem ser expostas ao háfnio por um curto período de tempo, mesmo em temperatura ambiente; a 35 ° C, taxas de remoção de mais de 3 mm / ano devem ser esperadas. Em bases aquosas é resistente até uma temperatura de aproximadamente 100 ° C, a remoção de material é geralmente inferior a 0,1 mm / ano.
isótopo
Há um total de 35 isótopos e 18 isômeros nucleares de háfnio 153Hf para 188Hf conhecido. O háfnio natural é um elemento misto que consiste em um total de seis isótopos diferentes. O isótopo mais comum é com uma frequência de 35,08% 180Hf segue 178Hf com 27,28%, 177Hf com 18,61%, 179Hf com 13,62%, 176Hf com 5,27% e 174Hf a 0,16%. Como o único isótopo natural é 174Hf fracamente radioativo, é um emissor alfa com meia-vida de 2 x 1015 Anos. Os isótopos 177Hf e 179Hf pode ser detectado com o auxílio de espectroscopia de NMR.
O isômero principal 178 2mCom meia-vida de 31 anos, o Hf é longo e ao mesmo tempo emite forte radiação gama de 2,45 MeV quando decai. Esta é a energia mais alta emitida por um isótopo estável por um longo período de tempo. Uma aplicação possível é usar este isômero central como fonte de lasers poderosos. Em 1999, Carl Collins descobriu que o isômero pode liberar sua energia de uma só vez quando exposto aos raios-X. No entanto, possíveis aplicações, como explosivos, são improváveis.
Usar
Chapa de háfnio a partir de resíduos industriais
Por ser difícil de extrair, o háfnio é usado apenas em pequenas quantidades. A principal área de aplicação é a tecnologia nuclear, na qual o háfnio é usado como uma haste de controle para regular a reação em cadeia em reatores nucleares. O uso de háfnio tem várias vantagens sobre outras possíveis substâncias absorvedoras de nêutrons. O elemento é muito resistente à corrosão e a reação nuclear com os nêutrons cria isótopos de háfnio, que também possuem seções transversais de alta absorção. Devido ao alto preço, muitas vezes só é adequado para aplicações militares, por exemplo, para reatores em submarinos atômicos.
Existem alguns outros usos. O háfnio reage rapidamente com pequenas quantidades de oxigênio e nitrogênio e pode, portanto, ser usado como uma substância absorvente para remover as menores quantidades dessas substâncias de sistemas de ultra-alto vácuo. Quando queimado, o metal emite uma luz muito brilhante. Portanto, é possível usar háfnio em lâmpadas de flash com uma eficiência luminosa particularmente elevada. Vários compostos muito estáveis e de alto ponto de fusão, especialmente nitreto de háfnio e carboneto de háfnio, podem ser feitos a partir dos elementos.
Em ligas com metais como nióbio, tântalo, molibdênio e tungstênio, uma adição de 2% de háfnio aumenta a resistência. São criados materiais particularmente estáveis, de alto ponto de fusão e resistentes ao calor.
segurança
Como muitos outros metais, o háfnio é altamente inflamável e pirofórico em seu estado finamente dividido. Por outro lado, em estado compacto não é inflamável. O metal não é tóxico. Por essas razões, nenhuma regulamentação especial de segurança precisa ser observada ao manusear háfnio.
Conexões
O háfnio forma vários compostos. Estes são principalmente sais ou cristais mistos e geralmente têm pontos de fusão elevados. O estado de oxidação mais importante do háfnio é + IV, mas os compostos em estados de oxidação mais baixos, de 0 a + III, e em complexos também são conhecidos estados de oxidação negativos.
óxido (IV) de háfnio
O óxido de háfnio (IV) é um sólido muito estável e de alto ponto de fusão. Tem uma permissividade relativa elevada de 25 (para comparação: dióxido de silício: 3,9). Portanto, ele pode ser usado como um dielétrico de alto k para isolar a conexão de controle (porta) para microprocessadores. Ao reduzir ainda mais as larguras das estruturas, as correntes de fuga estão se tornando um problema cada vez maior, porque a miniaturização das estruturas CMOS também requer isolamentos de porta mais finos. A corrente de fuga indesejada aumenta acentuadamente abaixo de 2 nm devido ao efeito túnel. Ao usar um dielétrico de alto k, a espessura do dielétrico pode ser aumentada novamente a fim de reduzir a corrente de fuga sem que o transistor tenha uma perda de desempenho (redução na velocidade de chaveamento). Assim, dielétricos mais espessos permitem uma maior miniaturização.
Outros compostos de háfnio
O carboneto de háfnio é uma das substâncias com maior ponto de fusão. Junto com o nitreto de háfnio e o boreto de háfnio, é um dos materiais duros.
Existem alguns compostos halógenos conhecidos de háfnio. No estado de oxidação + IV existem fluoreto e cloreto, brometo e iodeto. O cloreto de háfnio (IV) e o iodeto de háfnio (IV) desempenham um papel na produção de háfnio. Nos estados de menor oxidação, apenas são conhecidos compostos de cloro e bromo e iodeto de háfnio (III).
O hexafluoridoafonato de potássio (IV) K2[HFF6], bem como o hexafluoridoafonato de amônio (IV) (NH4)2[HFF6] pode ser usado para separar o háfnio do zircónio, uma vez que ambos os sais são mais solúveis do que os correspondentes complexos de zircónio.
| Geral | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome, símbolo, número atômico | Háfnio, Hf, 72 | ||||||||||||||||||||||||||||||||||||||||||||||||
| série | metais de transição | ||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloco | 4, 6, d | ||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | cinza aço | ||||||||||||||||||||||||||||||||||||||||||||||||
| número CAS | 7440-58-6 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Fração de massa da concha de terra | 4,2 ppm | ||||||||||||||||||||||||||||||||||||||||||||||||
| nuclear | |||||||||||||||||||||||||||||||||||||||||||||||||
| massa atômica | 178,49 u | ||||||||||||||||||||||||||||||||||||||||||||||||
| Raio atômico (calculado) | 155 (208) pm | ||||||||||||||||||||||||||||||||||||||||||||||||
| Raio covalente | 150 pm | ||||||||||||||||||||||||||||||||||||||||||||||||
| configuração electrónica | [Xe] 4f14 5d2 6s2 | ||||||||||||||||||||||||||||||||||||||||||||||||
| 1. ionização | 658,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 2. ionização | 1440 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 3. ionização | 2250 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| 4. ionização | 3216 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| fisicamente | |||||||||||||||||||||||||||||||||||||||||||||||||
| estado físico | fest | ||||||||||||||||||||||||||||||||||||||||||||||||
| modificações | dois (α- / β-Hf) | ||||||||||||||||||||||||||||||||||||||||||||||||
| estrutura de cristal | hexagonal | ||||||||||||||||||||||||||||||||||||||||||||||||
| densidade | 13,28 g / cm3 (25 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| dureza de Mohs | 5,5 | ||||||||||||||||||||||||||||||||||||||||||||||||
| magnetismo | paramagnético ( = 7,0 10-5) = 7,0 10-5) |
||||||||||||||||||||||||||||||||||||||||||||||||
| ponto de fusão | 2506 K (2233 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| ponto de ebulição | 4876 K (4603 ° C) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molar | 13,44 · 10-6 m3/ mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| Calor de vaporização | 630 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| calor de fusão | 25,5 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||
| pressão de vapor | 0,00013 Pa em 1970 K | ||||||||||||||||||||||||||||||||||||||||||||||||
| velocidade do som | 3010 m / s em 293,15 K | ||||||||||||||||||||||||||||||||||||||||||||||||
| Capacidade de calor específico | 140 J / (kg · K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade elétrica | 3,12 · 106 A / (v · m) | ||||||||||||||||||||||||||||||||||||||||||||||||
| condutividade térmica | 23 W / (m K) | ||||||||||||||||||||||||||||||||||||||||||||||||
| Químico | |||||||||||||||||||||||||||||||||||||||||||||||||
| estados de oxidação | 4 | ||||||||||||||||||||||||||||||||||||||||||||||||
| potencial normais | -1,505 V (HfO2 + 4 H.+ + 4 e- → Hf + 2 H2O) |
||||||||||||||||||||||||||||||||||||||||||||||||
| eletronegatividade | 1,3 (escala de Pauling) | ||||||||||||||||||||||||||||||||||||||||||||||||
| isótopo | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| propriedades de RMN | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||
| segurança | |||||||||||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||||||||||



